Clinical trials in Republic of Belarus
白俄罗斯国家概况
作为临床试验的地点,白俄罗斯可以为制药公司提供很多有价值的东西。白俄罗斯,正式名称为白俄罗斯共和国,是东欧的一个国家。白俄罗斯是欧洲第13大和第20大人口大国,人口为920万。由于人口众多,白俄罗斯的竞争性试验并不饱和,这对临床试验赞助商来说是一个机会。
白俄罗斯的医生和医院提供的医疗服务高于平均水平,超过了欧盟国家达到的平均水平。该国每1,000名居民拥有10. 8张医院病床。全球平均水平是2. 9张病床。在欧盟内部,每1000名居民有4. 6张病床。总体而言,白俄罗斯的医生密度在这一时期有所提高。在白俄罗斯,每10,000名居民大约有41名医生。
白俄罗斯的医生都受过严格的培训,并有动力担任主要研究人员(PI)。他们的英语水平达到中级或高级,并接受过GCP的培训。
白俄罗斯特别适合肿瘤学、心脏病学、风湿病学和移植方面的试验,因为明斯克是专门从事这些领域的大型共和国科学中心的所在地。这些中心设备精良,配备了在进行临床试验方面经验丰富的临床医生,并且可以访问潜在试验参与者的广泛的病人数据库。
白俄罗斯提供全民医疗保健。这意味着大多数人都可以获得许多免费的医疗保健服务。白俄罗斯卫生部正在努力改善该国所有公民的医疗服务的可用性和质量,没有例外,主要是通过门诊医疗机构。白俄罗斯仍然致力于普及医疗服务的原则,通过主要是国有设施按地域分层组织的方式免费提供医疗服务。城市地区的区域诊所和共和国中心以及农村地区的门诊部提供医疗保健。农村病人在必要时被转到城市中心进行进一步咨询和治疗。在大多数情况下,病人必须在检查后由全科医生转诊给专家。这意味着,白俄罗斯的病人流向是可预测的,病人集中在大医院,这对临床试验是有利的。
药品保险通常只限于最便宜的产品 – 通常是本地药品或廉价的仿制药。这种情况导致有很高比例的病人没有接触过最新的医药进展,他们渴望获得通过临床试验提供的突破性治疗。他们认识到,这个过程为他们提供了比其他方式更密集的医疗服务。试验参与者可以获得最新的治疗进展(而不是当地的仿制药),并在PI的持续监督下从额外的检查和测试中受益。
该国有很高比例的病人没有接触过现代治疗方法;这是一个可以识别出无药可救的病人的国家。
白俄罗斯的城市人口约为79.91%。最大的城市是明斯克、戈梅利、莫吉廖夫和维捷布斯克。在白俄罗斯,没有必要在许多城市启动研究点来招募病人。
根据世界银行的数据,2019年白俄罗斯成人和青年的识字率达到99.9%。这意味着ICF程序被患者充分理解。
白俄罗斯的生活成本相对较低。明斯克的平均月薪为500美元。这对临床试验申办者来说意味着巨大的节省。
白俄罗斯的临床试验情况
根据clinicaltrials.gov的数据,在白俄罗斯有333项试验,截至2013年4月4日,其中90项正在进行。
根据白俄罗斯临床试验登记处的数据,自2001年以来共有1377项试验。按阶段的分布情况如下:
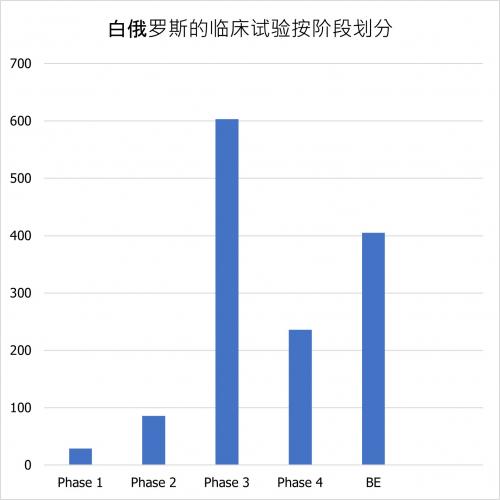
根据上表所示,530项试验是由白俄罗斯制药公司进行的国家试验,417项是由国际公司在白俄罗斯进行的临床试验。其中,430项是多中心试验。
白俄罗斯的监管情况
在白俄罗斯共和国进行临床试验的关键文件是白俄罗斯共和国卫生部2020年11月6日颁布的《医药产品临床试验条例》#94。
临床试验由卫生部的决定批准,在这之前要进行一系列与共和国单一制企业 "医疗保健专业知识和测试中心 "进行的专家检查有关的初步技术工作;由医疗保健组织的独立伦理委员会批准临床试验,在此基础上计划进行临床试验。准备工作的总时间不得超过120个自然日。经双方同意,这一期限可延长至360个自然日。 根据初步审查的结果,该中心就是否存在(不存在)卫生部颁发临床试验许可证的理由出具结论。然后将结论提交给伦理委员会,医疗机构的伦理委员会对提交的文件、材料和信息进行专家评估,并根据申请人与医疗机构达成的协议,对调查人员的资格和医疗机构是否具备按照良好临床实践要求进行临床试验的条件进行评估。医疗机构伦理委员会的专家评估和出具批准进行临床试验的结论,应按照关于通过本条例的决议批准的《独立伦理委员会条例》规定的程序和条件进行。
此外,为获得进行临床试验的批准,申请人应在初步审查和专家评估后向卫生部提出申请。中心应在征得申请人书面同意后,让卫生部查阅申请人之前提交给中心的一系列初步工作的文件。卫生部根据对申请的审查结果作出决定。
在获得进行临床试验的批准后,申办者与卫生部批准书和临床试验方案中规定的医疗机构签订合同。
医药产品的临床试验只能在卫生部指定的医疗机构进行。
由于白俄罗斯是欧亚经济联盟的成员,它遵循欧亚经济联盟的临床试验准则。在欧洲经济联盟注册的临床试验是按照欧洲经济联盟的要求进行的。还需要注意的是,在EAEU注册药品可能需要病人在该联盟的某个成员国注册。EAEU的其他国家有俄罗斯、亚美尼亚、哈萨克斯坦、亚美尼亚、吉尔吉斯斯坦。
白俄罗斯的临床试验质量
在白俄罗斯,通常需进行2次FDA检查。两次检查的结果都需是NAI。无行动指示(NAI)意味着在检查过程中没有发现不良条件或做法(或发现的不良条件没有理由采取进一步的监管行动)。这意味着白俄罗斯的临床试验是在高质量的水平上进行的。
摘要:白俄罗斯的临床试验
在临床试验方面,白俄罗斯是一块隐藏的宝石。这个国家可以提供一些优势:
·
由于病人的积极性很高,四分之三的病人生活在城市中心(这个比例与法国和德国相似),因此入学率很高。
·
一个中等规模的、对现代治疗持开放态度的无毒品人群。
·
有一大批热情的、讲英语的医生,他们在临床研究方面的经验是不断发展的。
·
受过高等教育、训练有素的医务人员,他们熟悉良好临床实践(GCP)(监管标准),符合美国食品和药物管理局(FDA)和欧洲药品管理局(EMA)的要求。
·
与其他地区相比,整体成本结构是有利的。
·
白俄罗斯拥有确保病人安全、优质数据和高效运作的临床基础设施。
·
透明的监管要求
Smooth Drug Development -- 白俄罗斯的一家CRO公司
作为一个值得信赖的生物制药合作伙伴,我们在高招聘率国家拥有全方位的研究能力。我们在欧洲、独联体、欧亚经济联盟和印度提供全方位的临床试验服务。我们通过快速、高效和具有成本效益的患者招募,确保客户满意。Smooth
Drug Development公司在白俄罗斯有运营。我们能够在白俄罗斯进行临床试验,或将白俄罗斯的站点纳入全球试验。
